薬剤師のためのBasic Evidence(大腸癌編)Vol. 1
掲載日:2022年5月9日

加藤 健 先生
国立がん研究センター中央病院
消化管内科、頭頸部・食道内科 科長
本邦における結腸と直腸を合わせた大腸癌の罹患数は、2018年現在、男性で前立腺癌、胃癌に続き第3位、女性で乳癌に続き第2位です。また、死亡数は2019年現在、男性で第3位、女性で第1位と、罹患数、死亡数ともに高い割合を占めています1)。
大腸癌の治療は、内視鏡治療、手術治療、薬物療法、放射線療法の4つに大別され、病期(Stage)や他の臓器への転移の有無、全身状態、年齢、併存疾患などを考慮して決定されます。
内視鏡や手術による治療は根治を目標とし、切除可能な大腸癌が対象となります。
薬物療法には、術後の再発抑制を目的とした術後補助化学療法と、腫瘍の進行抑制による延命、症状のコントロールを目的とした切除不能進行・再発大腸癌に対する薬物療法があります(表1)。「薬剤師のためのBasic Evidence(大腸癌編)」では、これらの薬物療法の基礎的な内容を取り上げて解説します。
薬剤師の皆さんには、薬物療法による標準的な治療方針や薬剤について積極的に学んでいただき、患者さんへの服薬指導などに生かしていただきたいと思います。
表1 大腸癌の薬物療法


平野 秀和 先生
国立がん研究センター中央病院
消化管内科
「薬剤師のためのBasic Evidence(大腸癌編)」vol. 1では、大腸癌の薬物療法の概要がつかめるよう、大腸癌薬物療法の変遷、本年改訂された「大腸癌治療ガイドライン 医師用2022年版」に準拠した「切除不能進行・再発大腸癌に対する薬物療法」の基礎的な内容をご紹介します。また、薬剤の種類による大まかな副作用の違いについても示していますので、ぜひ患者さんへのご指導に役立てていただきたいと思います。
- 国立がん研究センター:がん情報サービス 最新がん統計
https://ganjoho.jp/reg_stat/statistics/stat/summary.html(2022年1月閲覧)
大腸癌の薬物療法の変遷
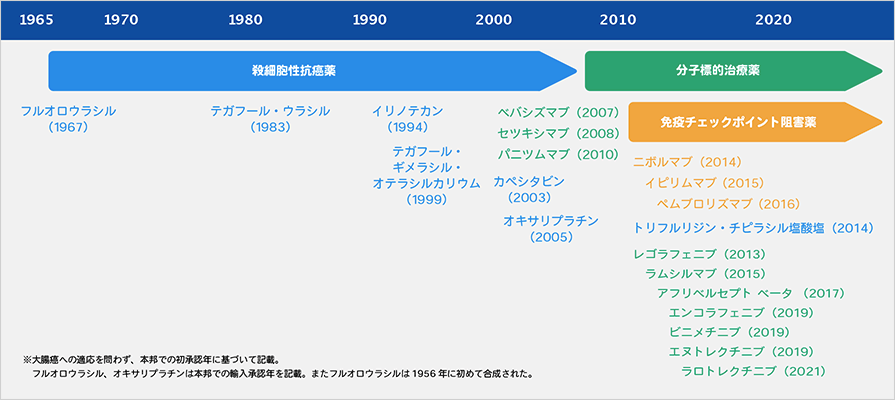
切除不能進行・再発大腸癌の薬物治療は1956年のフルオロウラシルの登場を機に、約半世紀にわたりフルオロウラシルが中心的な役割を担ってきました(図1)。その後、1994年にイリノテカン、2005年にオキサリプラチンが承認され、2000年代にはフッ化ピリミジン系抗癌薬(フルオロウラシル、カペシタビン、テガフール・ギメラシル・オテラシルカリウムなど)とオキサリプラチンまたはイリノテカンを組み合わせたFOLFOX療法、FOLFIRI療法などの多剤併用療法が確立しました。
近年では、これらの殺細胞性抗癌薬の組み合わせに、ベバシズマブ、セツキシマブ、パニツムマブいずれかの分子標的治療薬を加えた治療が主流となってきており、「大腸癌治療ガイドライン 医師用2022年版」でも切除不能な大腸癌に対する一次治療として強く推奨されています。
さらに、免疫チェックポイント阻害薬であるペムブロリズマブ、ニボルマブ±イピリムマブも高頻度マイクロサテライト不安定性(MSI-H)を有する治癒切除不能な進行・再発結腸・直腸癌に対する適応が追加となり、薬物療法は新たな時代を迎えています。
薬物療法の進歩に伴い、治療成績も向上し、薬物療法を実施しない場合は生存期間中央値が約8ヵ月との報告があるのに対し1)、薬物療法により30ヵ月を超えるまでになりました2)。また、従来は入院治療が行われていましたが、副作用の少ない抗癌薬の開発や副作用に対する有効な支持療法の確立により通院治療が可能になり、患者さんのQOLの向上に寄与しています。
図1 大腸癌治療に用いられる主な抗癌薬開発の歴史※
- Simmonds PC: BMJ. 2000; 321(7260): 531-535.
-
Yamada Y, et al.:Lancet Oncol. 2013; 14(13): 1278-1286.
Loupakis F, et al.:N Engl J Med. 2014; 371(17): 1609-1618.
Yamazaki K et al.: Ann Oncol. 2016(27): 1539-1546.
薬物療法の適応
図2に「大腸癌治療ガイドライン 医師向け2022年版」に掲載されている一次治療の方針を決定する際のプロセスを示します。なお、これらの推奨されるレジメン以外を選択することも可能であり、実臨床では患者さんの状態などを考慮して最適な治療が選択されます。
1)適応の可否を判断
切除不能進行・再発大腸癌に対する薬物療法を検討する際は、まず適応の可否を判断します。
薬物療法が適応となる患者さんは、病理組織診断で結腸または直腸の腺癌であることが確認されており、治癒切除不能と診断されていることが前提となります。加えて、全身・主要臓器機能の状態や重篤な併存疾患の有無によりFit、Vulnerable(Vul)、Frailの三つに分類されます。全身状態が良好で、主要臓器機能が保たれ、重篤な併存疾患がないなど、一次治療のオキサリプラチン、イリノテカンや分子標的治療薬の併用療法に対して、忍容性に問題がないと判断される患者さんはFit、忍容性に問題があると判断される患者さんはVulとなり、薬物療法の適応が検討されます。一方で、これらの条件を満たさず薬物療法の適応とならないFrailの患者さんでは、対症療法(best supportive care:BSC)が選択されます。
2)遺伝子検査と腫瘍占拠部位による治療薬の選択
薬物療法が適応可能と判断されたら、一次治療開始前にRAS(KRAS/NRAS)遺伝子検査、BRAFV600E遺伝子検査、MSI検査を行います※。
薬物療法が適応可能なFitまたはVulのうち、MSI-H陽性例では、ペムブロリズマブが選択されます。
MSI-H陰性例では、RAS、BRAF遺伝子変異の有無、腫瘍占居部位、 Fit・Vulのどちらであるかにより推奨されるレジメンが異なります。
Fitの場合、RAS/BRAF野生型で左側大腸癌(下行結腸、S状結腸、直腸)の患者さんにはFOLFOXまたはFOLFIRIに抗EGFR抗体薬(セツキシマブまたはパニツムマブ)併用療法、RAS/BRAF野生型の右側大腸癌(盲腸、上行結腸、横行結腸)の患者さん、またはRAS、BRAF遺伝子のどちらかに変異を持つ患者さんにはDoublet(FOLFOX、CAPOX、SOX、FOLFIRI、S-1+IRI)またはTriplet(FOLFOXIRI)とベバシズマブの併用療法が選択されます。
Vulの場合、上記のFitで用いたFOLFOX、FOLFIRIなどのオキサリプラチンやイリノテカンの多剤併用療法をフッ化ピリミジン系抗癌薬(5-FU+l-LV、UFT+LVなど)単独療法に置き換え、適応となる場合は、ベバシズマブの併用が推奨されています。
※本邦において、切除不能大腸癌患者さんの約50%にRAS遺伝子変異、約5%にBRAFV600E遺伝子変異、約4%にMSI-Hが認められると報告されています。
レジメンの名称は、使用する薬剤名の一部または略号で成り立っています。代表的なレジメンを以下に示します。
- FOLFOX:フルオロウラシル(5-FU) +レボホリナート(LV/l-LV)+オキサリプラチン(OX)
- CAPOX:カペシタビン(Cape)+オキサリプラチン
- SOX:テガフール・ギメラシル・オテラシルカリウム(S-1)+オキサリプラチン
- FOLFIRI:フルオロウラシル+レボホリナート+イリノテカン(IRI)
- FOLFOXIRI:フルオロウラシル+レボホリナート+オキサリプラチン+イリノテカン
- 5-FU+l-LV:フルオロウラシル+レボホリナート
- UFT+LV:テガフール・ウラシル(UFT) +レボホリナート
図2 一次治療の方針を決定する際のプロセス

切除不能進行・再発大腸癌に対する
薬物療法のアルゴリズム
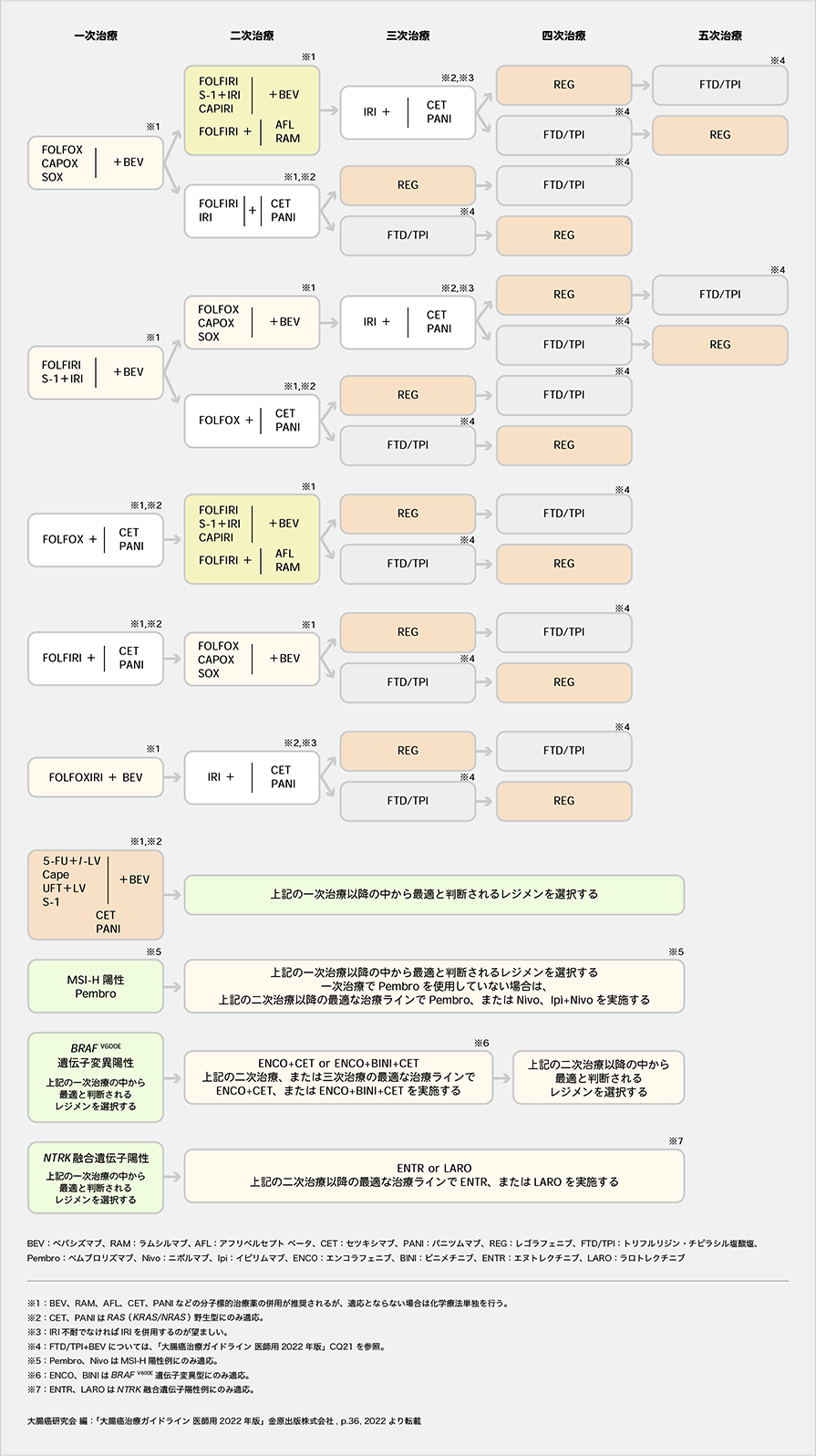
「大腸癌治療ガイドライン 医師用2022年版」では、切除不能進行・再発大腸癌に対して、図3のようなアルゴリズムが示されています。
臨床試験において有用性が示されており、かつ保険診療として国内で使用可能な一次治療のレジメンを表2に示します。殺細胞性抗癌薬として、フッ化ピリミジン系抗癌薬にオキサリプラチン、イリノテカン、またはその両方を用い、分子標的治療薬(ベバシズマブ、セツキシマブまたはパニツムマブ)を組み合わせたレジメンが選択されることが多いですが、Vul例では、オキサリプラチンやイリノテカンを用いないレジメンが選択されることもあります。
オキサリプラチンを含むレジメンで一次治療が無効だった場合は、二次治療ではイリノテカンを含むレジメンに変更します。逆の場合も同様に、二次治療では一次治療と異なる薬剤が選択されます。
また、三次治療以降ではレゴラフェニブやトリフルリジン・チピラシル塩酸塩などの経口抗癌薬を用いた後方治療が選択されます。
薬剤師のためのBasic Evidence(大腸癌編)Vol.2では、このアルゴリズムの一次治療のレジメンのうち、当院でよく用いるレジメンについて、有効性の根拠となった臨床試験に基づき、解説します。
表2 代表的な一次治療レジメンの組み合わせ

図3 切除不能進行・再発大腸癌に対する
薬物療法のアルゴリズム
薬物療法における副作用
薬物療法による副作用は、薬剤の作用機序によりさまざまな症状が現れます。
殺細胞性抗癌薬は癌細胞を攻撃するとともに正常な細胞をも破壊するため、血液障害や消化器症状、臓器障害、皮膚・神経症状など発現する副作用は多岐にわたります。
分子標的治療薬では皮膚や爪の異常、高血圧、出血など、従来の殺細胞性抗癌薬とは異なる副作用が起こります。
免疫チェックポイント阻害薬では、免疫反応が過剰になり、皮膚やさまざまな臓器に炎症性の免疫反応が現れる免疫関連有害事象(immune-related Adverse Events:irAE)という特徴的な副作用があります。
致死的な副作用の予防や症状軽減はもちろんのこと、生命に関わらなくとも治療の中止やQOL低下を招く副作用症状をコントロールすることも重要です。
各レジメンで使用される薬剤による副作用を理解し、それぞれの症状や発現時期に応じた支持療法を行うことが、安全な薬物療法の継続につながります。支持療法については、本Webサイト掲載の「診療現場最前線」もご参考ください。
薬剤師の皆さんへ

薬剤師の皆さんが各疾患の基本的な治療方針を理解することはとても重要です。
治療方針を知ることで、注意すべき副作用を想定しながら服薬指導にあたることができます。
大腸癌の薬物療法では、カペシタビンやS-1、レゴラフェニブなどの経口抗癌薬や支持療法に使用される薬剤が院外処方となることがあります。経口抗癌薬はレジメンによって休薬期間などが異なるため、服薬指導を行う保険薬局薬剤師も治療方針やレジメンを理解していることが重要です。支持療法に使われる薬剤については、その処方目的を知ることで副作用症状をより的確にモニタリングすることができます。
ぜひ、この「薬剤師のためのBasic Evidence」を使って勉強してみてください。
当コンテンツの情報および監修者の所属・役職は掲載日時点での情報となります。
また、当該医薬品の使用に当たっては、最新の添付文書、ガイドライン等をあわせてご参照くださいますようお願いします。