薬剤師のためのBasic Evidence
(腎障害編:シスプラチンによる急性腎障害)
掲載日:2023年10月6日

玉木 慎也 先生
KKR札幌医療センター
薬剤科 薬剤科長
治験管理センター 副センター長
がん薬物療法は近年、分子標的薬や免疫チェックポイント阻害薬の登場により劇的に変化をとげました。一方、こうした状況において、細胞障害性抗がん薬に分類できるシスプラチンは、本邦で承認されてからすでに40年が経過したものの、現在でも標準治療として多くのレジメンに組み込まれています。
シスプラチンは非小細胞肺癌、頭頸部癌、食道癌、子宮頸癌、卵巣癌など幅広いがん種に抗腫瘍効果を示す白金製剤です。しかしながら、本剤の副作用として、腎障害、悪心・嘔吐、聴力障害、末梢神経障害、骨髄抑制などの副作用が知られていますが、中でも腎障害は用量制限毒性となる重要な副作用です。
そこで、腎障害※を予防するため、本剤を投与する際には、大量補液、利尿薬の併用、マグネシウムの補充が日常診療で広く行われています。また、補液量を少なくするショートハイドレーション法も外来化学療法で行われています。
「薬剤師のためのBasic Evidence(腎障害編:シスプラチンによる急性腎障害)」では、2022年に改訂された「がん薬物療法時の腎障害診療ガイドライン 2022」に準拠した、本剤による腎障害の概要や予防について基礎的な内容を解説します。
※本編で紹介する腎障害は急性腎障害のことを言います。
目次
各製剤の詳細は電子添文をご参照ください。
シスプラチンについて
シスプラチンは、中心にある白金にそれぞれ2つのアンモニア分子と塩素イオンが結合した白金製剤で、2つのアンモニア分子が白金に対して同じ側に結合しているシス型化合物です(表1)。がん細胞内のDNA鎖と結合し、DNAの複製や転写によるアポトーシスの誘導によって抗腫瘍効果を示します。
本剤は1965年にRosenberg博士らが、細菌の増殖に対する電場の影響を検討していた際、白金電極から電解質溶液中に溶出した白金化合物による大腸菌の細胞分裂抑制作用を発見することにより端を発します1)。その後、種々の白金化合物の抗腫瘍効果についてスクリーニングが行われ、本剤が最も有望な抗腫瘍効果を示したことから抗悪性腫瘍剤として臨床開発が始まりました。ただし、1970年代前半に米国にて臨床試験が開始されたものの、強い腎毒性のために開発が一時中断されました。その後、動物モデルにおいて本剤投与時に大量の水分負荷(ハイドレーション)と利尿薬を投与することにより、腎障害が回避可能であることが示されたことから2)、臨床研究でも本剤の有効性および安全性が検証された結果、1978年に欧米において承認、本邦においても1983年に承認されました。現在では多くのがん種に対する効能・効果を有しています(表2)。
こうした開発の経緯から、腎障害を回避するための方策として、本剤投与時は大量の水分負荷(ハイドレーション)を原則とし、これに加えて利尿薬の併用などが一般的に行われるようになっています。
表1 シスプラチン
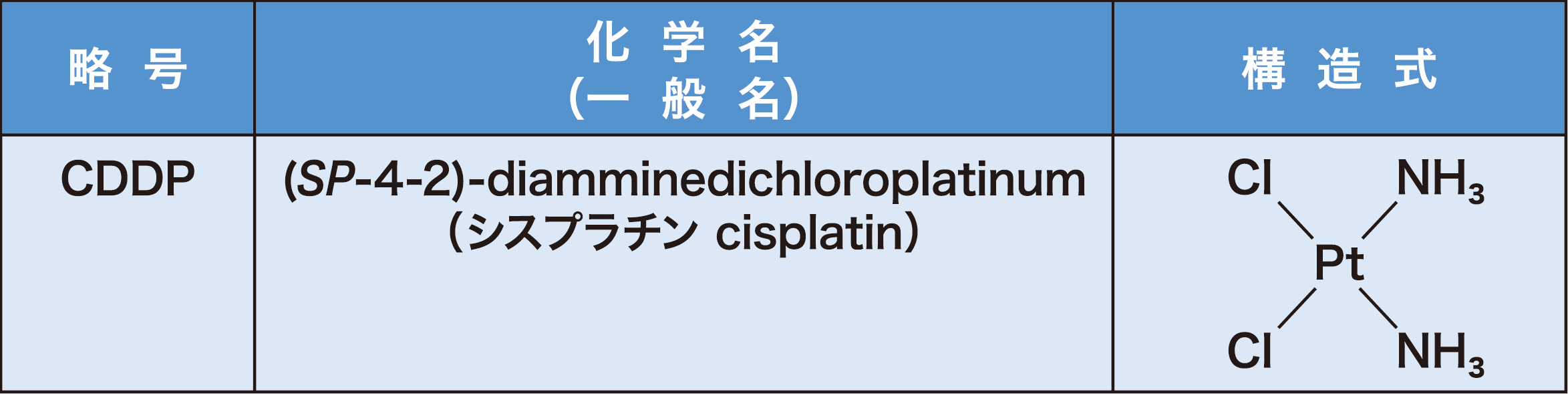
シスプラチン点滴静注10mg・25mg・50mg「マルコ」 インタビューフォーム(2022年3月改訂第11版)より作成
表2 シスプラチンの効能・効果

シスプラチン点滴静注10mg・25mg・50mg「マルコ」 添付文書(2022年3月改訂第22版)より作成
1)ROSENBERG B, et al.: Nature. 1965; 205:698-699.
2)Cvitkovic E, et al.: Cancer. 1977; 39 (4): 1357-1361.
シスプラチンによる腎障害
がん患者さんにおける腎障害の発症は生命予後に影響することが報告されています3)。さらに腎障害を起こした場合は、抗がん薬の中止や減量などの検討が必要になり、予定していた治療強度が保てなくなることによるがん自体の進行も、予後に影響を与える可能性があります。これらの点から、腎障害の予防は非常に重要と考えられています。
抗がん薬による腎障害の評価には、KDIGO(Kidney Disease Improving Global Outcomes)診断基準や有害事象共通用語規準(CTCAE)(表3)が用いられます。 KDIGO診療ガイドラインでは、急性腎障害は「48時間以内に血清クレアチニン値が0.3mg/dL以上上昇」、「7日以内に血清クレアチニン値が基礎値から1.5倍以上上昇」、「尿量0.5mL/kg/時未満が6時間以上持続」のいずれかで定義されています4)。
CTCAEは、全てのがん治療医が治療による有害事象を表現する共通した規準であり、治験を含む多くの臨床試験で使用されています。一方、KDIGO 診断基準は、腎臓専門医が治療介入する際に用いられています。
表3 CTCAEによる重症度評価(急性腎障害)
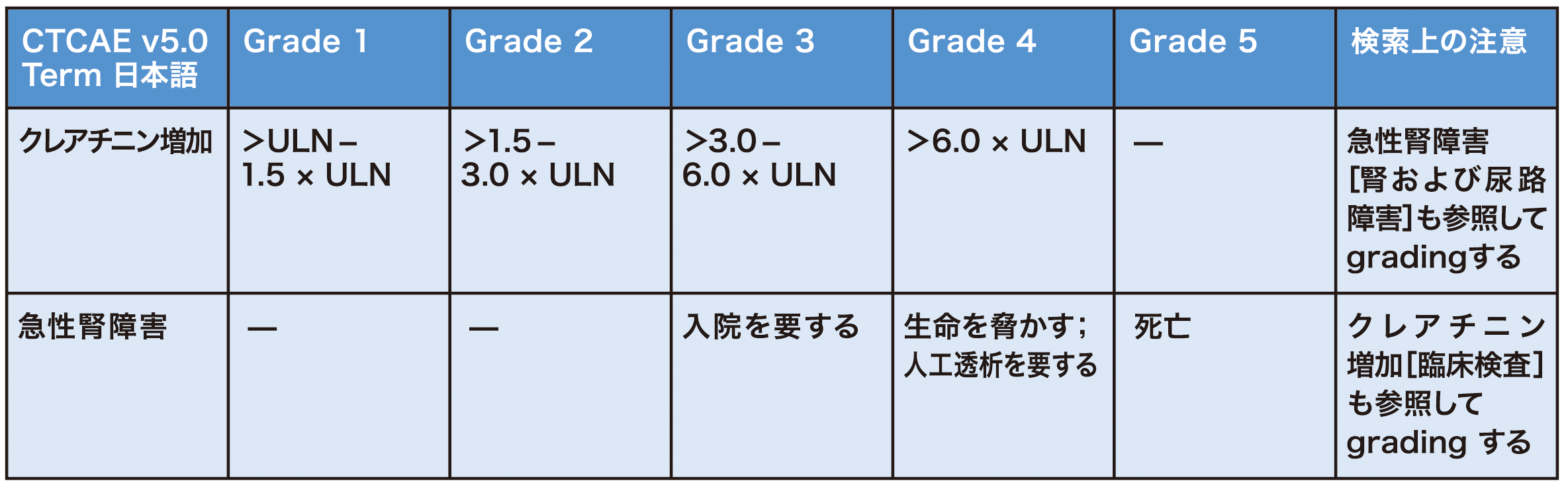
ULN:(施設)基準範囲上限
有害事象共通用語規準 v5.0 日本語訳JCOG版より引用、改変
JCOGホームページ http://www.jcog.jp(2023年7月閲覧)
抗がん薬の中でもシスプラチンは腎障害を起こしやすく、その頻度は20~30%と報告されています5,6)。また、本剤による腎毒性は用量依存性であり、非乏尿性の腎障害をきたしますが、多くは可逆性で、3~4週間以内に腎機能は回復します。ただし、本剤の総投与量が多い場合は、不可逆性の腎不全を呈する場合もあります7) 。
投与された本剤は約90%がアルブミンを主とする血漿蛋白と結合しますが、その他は非結合の遊離型シスプラチンとして存在します8)。蛋白結合型シスプラチンは糸球体で濾過されませんが、遊離型シスプラチンは糸球体で濾過されます。しかし遊離型には、糸球体で濾過されず尿細管分泌によって腎より排泄される場合もあります。その際に、近位尿細管の側底膜側に存在する有機カチオントランスポーター(OCT(organic cation transporter)2)を介して、能動的に細胞内に取り込まれ(図1)、尿細管上皮細胞内に蓄積し、DNAに直接結合して尿細管壊死を引き起こすことで腎障害が生じます9)。
本剤投与後、遊離型シスプラチンは約2時間程度で体内から排泄されます7)。本剤による腎障害を回避するためには、有害な遊離型シスプラチンの長時間にわたる腎での停滞を避け、速やかに排泄させる必要があります。そこで、腎毒性を軽減するために、大量の補液と必要に応じて利尿薬の投与が行われます。
一方、先ほど述べた通り、本剤による腎障害は非乏尿性であることが特徴です。シスプラチン排泄のために尿が出ているかの確認は必要ですが、尿量だけを確認しても腎障害を完全に否定することはできません。尿量の他に「浮腫」、「倦怠感」などの症状が認められた場合は腎障害を疑う必要があります。
本剤による腎障害の危険因子として、年齢、低アルブミン血症、心疾患、高血圧、本剤投与量などが報告されています9)。NSAIDsやレニン・アンジオテンシン系阻害薬を服用している患者さんでは腎血流低下による腎障害が起こりやすいので注意が必要です9)。
図1 近位尿細管におけるシスプラチンの取り込み
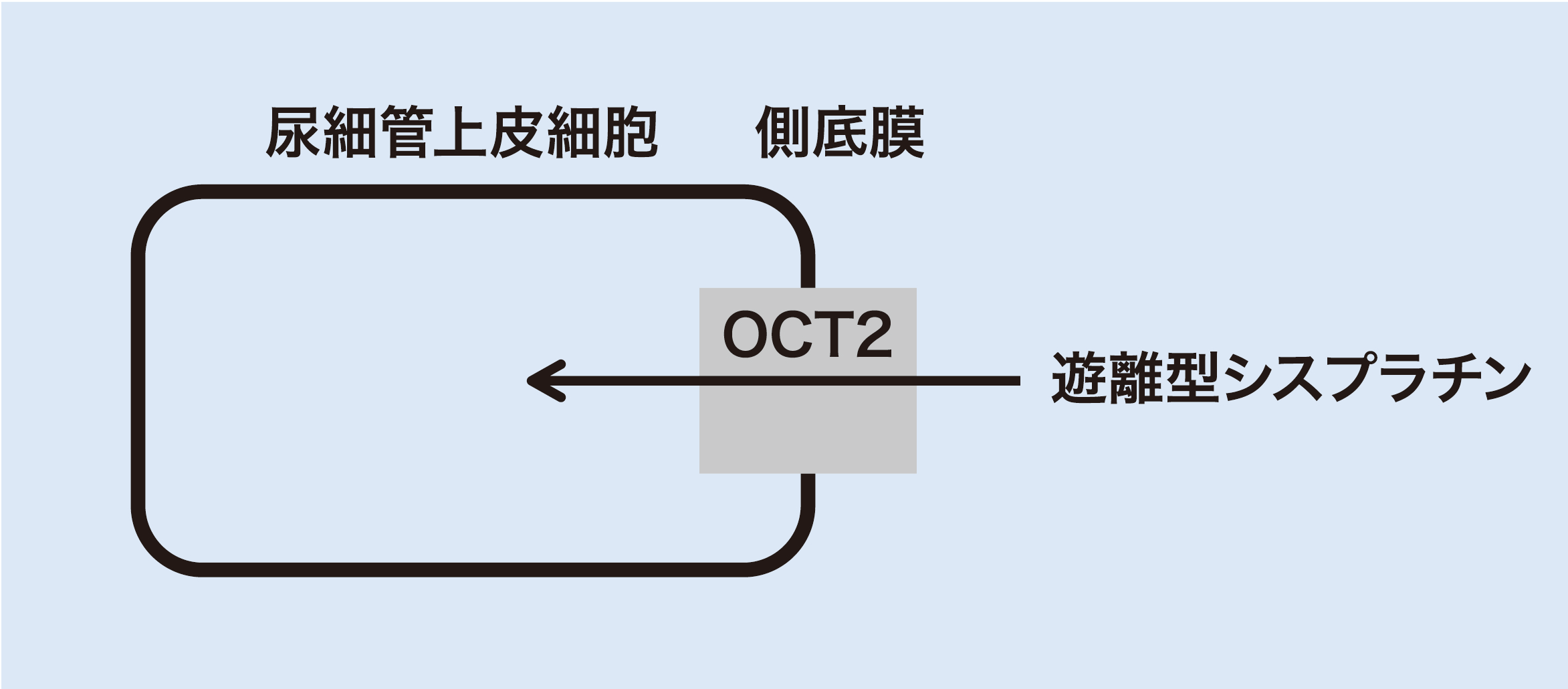
日本腎臓学会/日本癌治療学会/日本臨床腫瘍学会/日本腎臓薬物療法学会 編
「がん薬物療法時の腎障害診療ガイドライン 2022」 ライフサイエンス出版株式会社 より作成
3)Kang E, et al.: Cancer Med. 2019; 8(6): 2740-2750.
4)Kidney Disease: Improving Global Outcomes (KDIGO) Acute Kidney Injury Work Group
KDIGO Clinical Practice Guideline for Acute Kidney Injury. Kidney inter., Suppl. 2012; 2: 1–138.
5)Sato K, et al.: BMC Cancer. 2016; 16: 222.
6)Latcha S, et al.: Clin J Am Soc Nephrol. 2016; 11(7): 1173-1179.
7)伊與田 雅之, 他.: 昭和学士会誌. 2015; 75(4): 421-425.
8)堀内 正敏, 他.: 癌と化学療法. 1982; 9(4): 632-637.
9)日本腎臓学会/日本癌治療学会/日本臨床腫瘍学会/日本腎臓薬物療法学会 編
「がん薬物療法時の腎障害診療ガイドライン 2022」 ライフサイエンス出版株式会社
腎障害の予防
シスプラチンによる腎障害を軽減するため、3,000mL以上の補液とともに利尿薬投与やマグネシウム補充を行うことが「がん薬物療法時の腎障害診療ガイドライン2022」で推奨されています9)。本剤の添付文書においては、投与前後にそれぞれ4時間以上かけて1,000~2,000mLの補液を行うこと、および500~1,000mL以上の輸液に希釈した上で2時間以上かけて投与すること、投与中は尿量確保に注意し、必要に応じてマンニトールおよびフロセミド等の利尿薬を投与することが、腎毒性を軽減するための処置として、用法・用量に関する使用上の注意の項に記載されています10)。
利尿薬の投与については、その有効性と安全性を示すランダム化比較試験は行われていません。そのため、マンニトールとフロセミドのどちらを投与するのか、両方の薬剤を用いるのかについて明確な指針はなく、投与量についても報告によってさまざまであり一定の見解は示されていません。しかしながら、利尿薬の投与は開発早期から現在に至るまで広く用いられている方法であり、その有用性は確立していると考えられます9)。
また、本剤によって引き起こされる低マグネシウム血症も腎障害を悪化させる原因になります。本剤による低マグネシウム血症の原因は、尿細管障害による腎からのマグネシウム喪失とともに、本剤投与による嘔吐や下痢に伴う消化管からのマグネシウム喪失も関与しています。低マグネシウム血症時には近位尿細管に本剤が蓄積することで、腎障害が発現あるいは悪化することが示唆されています11)。
そのため、腎障害予防のためのマグネシウム投与は、添付文書には記載されていないものの、ガイドラインでは推奨されています9)。なお、本剤投与時の明確な推奨量はありませんが、臨床試験などにおいては本剤投与前に8mEqを補充する方法や、本剤投与前後にそれぞれ4mEqを補充する方法が用いられています9)。
なお、腎障害の予防や軽減を目的とした本剤の分割投与に関する前向きランダム化比較試験の結果は報告されておらず、分割投与法を積極的に推奨する根拠がありません。そのため、腎機能正常者に対する分割投与に関しては、有用性を示すエビデンスが乏しく推奨されません9) 。
10)シスプラチン点滴静注10mg・25mg・50mg「マルコ」 添付文書(2022年3月改訂第22版)
11)Yokoo K, et al.: Clin Exp Nephrol. 2009; 13(6): 578-584.
早期診断のためのバイオマーカー
腎障害の診断は、通常血清クレアチニン値に基づいて判定しますが、腎臓が障害されてから血清クレアチニン値が上昇するまでにタイムラグがあり、迅速な腎障害の診断・治療が困難となっていました。
そこで、血清クレアチニン値よりも早期に腎障害を検出するというコンセプトのもと、複数の新規バイオマーカーが開発されています。
シスプラチンにおいても腎障害の診断として、本剤投与3~4日後の血清クレアチニンの50%以上の増加を指標とすることが多い12)ものの、尿中バイオマーカーの測定により腎障害の発症を1日以上前に予測できるとの報告があり13)、腎障害の早期診断に有用であると示唆されています14)。
本邦では腎障害の早期診断バイオマーカーとして、尿中L-FABP(L型脂肪酸結合蛋白)と尿中NGAL(好中球ゼラチナーゼ結合性リポカリン)が保険収載されています。ただし、バイオマーカーのリアルタイム測定によってシスプラチンによる腎障害を早期診断することが腎予後や生命予後の改善につながるかどうかの検討はされていないため、 「がん薬物療法時の腎障害診療ガイドライン2022」ではバイオマーカーによる評価を弱く推奨する(提案する)としています9)
なお、当院においては本剤投与による腎障害の評価について、血清クレアチニンやeGFRによる評価が標準的に行われており、 ガイドラインに記載されているバイオマーカーの測定は日常的には行われていないのが現状です。
12)Abdelsalam M, et al.: BMC Nephrology. 2018; 19: 291.
13)Lin HY, et al.: Kaohsiung J Med Sci. 2013; 29: 304-311.
14)AKI(急性腎障害)診療ガイドライン作成委員会 編 「AKI(急性腎障害)診療ガイドライン2016」 東京医学社
ショートハイドレーション法
前項(腎障害の予防)で紹介した大量輸液法は、長時間に及ぶ輸液のために入院による管理を必要とすることから、がん薬物療法中の患者さんの生活の質(QOL)の低下に繋がる懸念があります。
こうした背景を踏まえ、従来の大量輸液法に比べ、少量かつ短時間の補液法である「ショートハイドレーション法」が行われています。ショートハイドレーション法は、全身状態が良好で、短時間の補液に耐えうる臓器機能を有している患者さんにおいて弱く推奨されています9)。
ショートハイドレーション法については当コンテンツで今後取り上げる予定です。

日本腎臓学会/日本癌治療学会/日本臨床腫瘍学会/日本腎臓薬物療法学会 編
「がん薬物療法時の腎障害診療ガイドライン 2022」 ライフサイエンス出版株式会社
シスプラチン点滴静注10mg・25mg・50mg「マルコ」 添付文書(2022年3月改訂第22版)
より作成
薬剤師の皆さんへ
シスプラチンは冒頭で述べた通り、幅広いがん種に抗腫瘍効果を示します。また、承認から40年経過しますが、いまなお標準治療における重要な薬剤の1つです。しかしながら、本剤による腎障害は用量制限毒性となる重要な副作用です。治療の継続ならびに治療強度を維持するためにも、本剤に伴う腎障害を念頭に置いた適切な管理が求められます。
本剤による腎障害の初期は自覚症状に乏しいことが多いですが、本剤投与を受けている患者さんで、尿量が減る、手や足がむくむ、体がだるいといった症状が現れる場合は腎障害が疑われますので、ただちに主治医に相談していただくといった指導が必要になります。
特に尿量低下は、患者さんご自身が把握しやすい症状となります。病院薬剤師は患者さんへの服薬指導を通して、保険薬局薬剤師はテレフォンフォローを通して、尿量の低下がないかは確認しておきたいポイントです。もし明らかな尿量の低下がみられた場合は、病院薬剤師であれば採血の依頼、保険薬局薬剤師であれば、ただちに病院に連絡する、あるいは患者さんへの受診勧奨など、早急な対応が必要となります。また、浮腫の増悪や著明な倦怠感の有無も併せて確認するのがよいと思います。さらに、シスプラチンによる悪心嘔吐の好発時期を過ぎてもなお継続する悪心・食欲不振についても、腎障害を疑う必要があります。
本剤は注射薬の催吐性リスク分類において高度催吐性リスクに分類されています15)。そのため、悪心・嘔吐が高頻度で発現すると予想され、これらの消化器毒性に伴う脱水によりさらに腎障害が増悪する可能性があることから、適切な制吐薬の投与も必要になります。制吐対策については、当コンテンツの「診療現場最前線:制吐療法」にてご確認ください。
15)日本癌治療学会 編「制吐薬適正使用ガイドライン2015年10月(第2版)
一部改訂版ver. 2.2」(2018年10月)
http://jsco-cpg.jp/item/29/index.html(2023年7月閲覧)
当コンテンツの情報および監修者の所属・役職は掲載日時点での情報となります。
また、当該医薬品の使用に当たっては、最新の添付文書、ガイドライン等をあわせてご参照くださいますようお願いします。
